La exitosa aplicación de la teoría cinética para el estado gaseoso se puede extender al resto de los estados de agregación de la materia tan solo utilizando los conceptos de distancia entre partículas y desplazamiento relativo:
- Si las partículas están juntas, su volumen no podrá variar. Así se explica el estado sólido y líquido, pero no el gaseoso, que es compresible.
- Si las partículas se desplazan entre ellas, su forma puede variar. Se explica así el comportamiento de los fluidos, como el estado líquido y el gaseoso.
7.1. Teoría cinética y cambios de estado
La teoría cinética no solo explica los estados de agregación de la materia, también es capaz de explicarnos cómo se producen los cambios de estado.
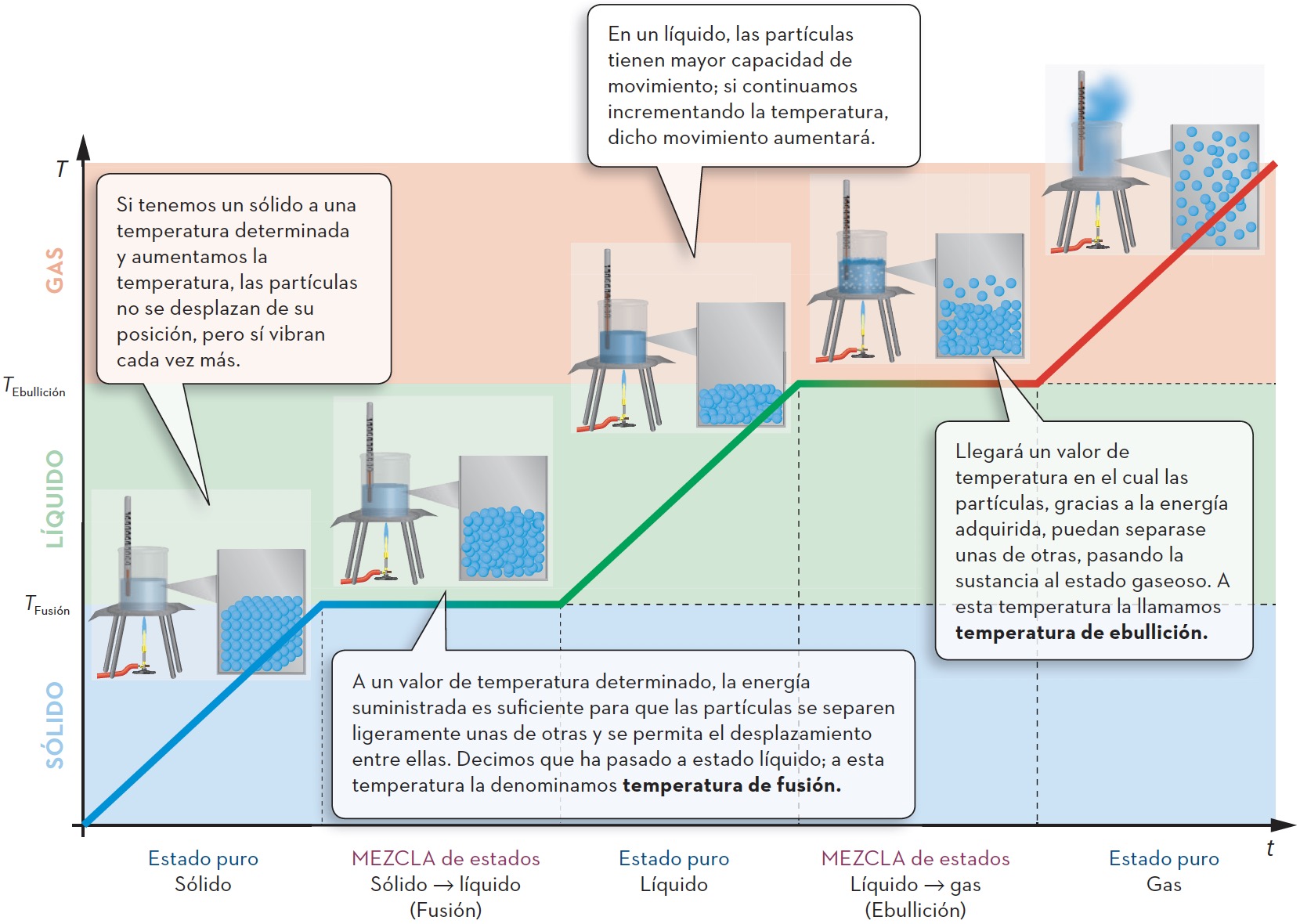
Recuerda que no debes confundir la evaporación y la ebullición:
- La evaporación es un fenómeno en el cual la superficie del líquido, a cualquier temperatura, se convierte en estado gaseoso.
- En la ebullición, sin embargo, todo el líquido pasa a estado gaseoso a una determinada temperatura.
7.2. Gráficas de cambio de estado
Las gráficas de cambio de estado suministran información sobre los cambios de estado que se producen como consecuencia de un proceso de calentamiento o enfriamiento y el tiempo empleado en producirse dichos cambios.
La siguiente imagen corresponde a una gráfica de enfriamiento desde el estado gaseoso hasta el estado sólido:
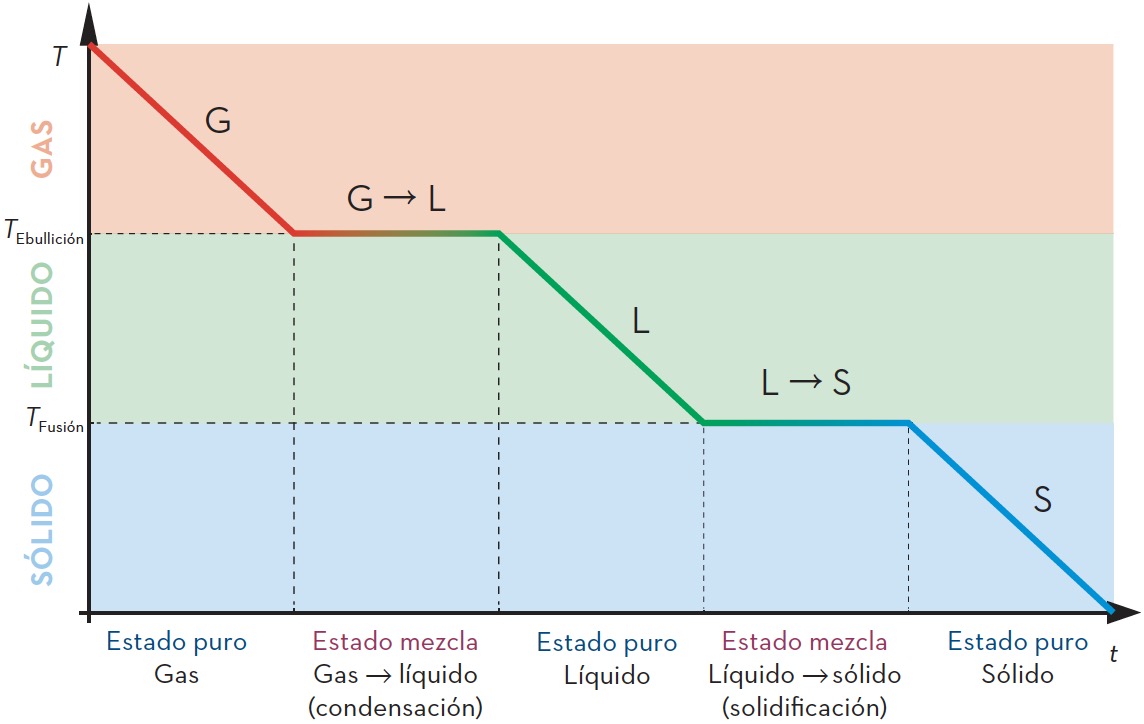
En ella, se observan una serie de tramos que podemos asimilar a:
- Estados puros (sólido, líquido y gaseoso): aquellos en los que al aplicar o eliminar calor la temperatura varía. Por tanto, en la gráfica aparecen como líneas inclinadas ascendentes o descendentes.
- Estados mezcla: corresponden a cambios de estados. En ellos la temperatura no varía y, por tanto, aparecen como una horizontal en la gráfica.
Los diferentes estados de agregación aparecen en orden creciente de la temperatura, de manera que se cumple:
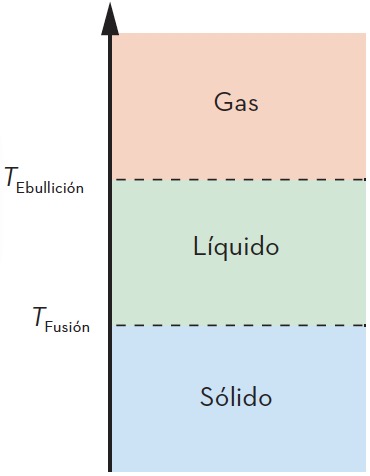
- Analiza la gráfica de la figura adjunta. Identifica los estados en los que se encuentra en cada instante considerando todas las posibles interpretaciones.
Solución
La gráfica presenta un solo tramo horizontal, por lo que estamos ante un único cambio de estado, pero no existe información sobre cuál es.
Existen, pues, dos posibilidades:
- Una condensación, desde el estado gaseoso al estado líquido.
- Una solidificación, desde el estado líquido al estado sólido.
