Los estudios de Schrödinger permitieron conocer qué orbitales hay en cada capa de la corteza del átomo:
- Capa 1. Solo orbital s.
- Capa 2. Orbitales s y p.
- Capa 3. Orbitales s, p y d.
- Capa 4 y siguientes. Orbitales s, p, d y f.
Para designar un orbital se indica el número de la capa y la letra del tipo, por ejemplo, 2s, 5p, etc.
Los orbitales del mismo tipo tienen la misma forma, aunque su tamaño es mayor cuanto mayor sea el número de la capa. Así, los orbitales 2s y 5s son esféricos, aunque el 5s es de mayor tamaño.
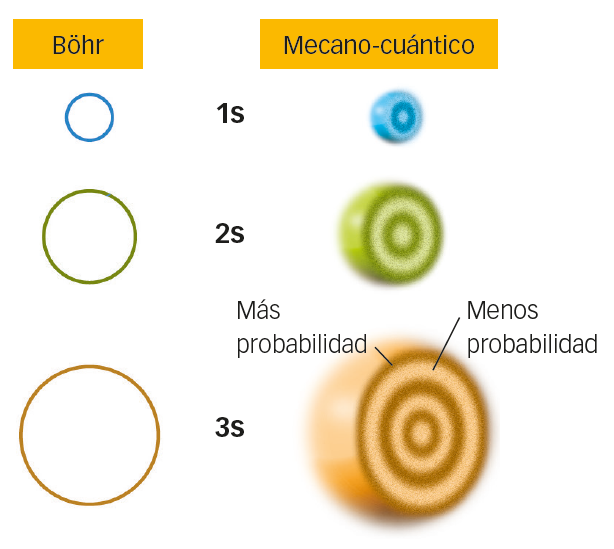
Comparación entre la órbita que describiría un electrón, según el modelo de Böhr, y el orbital, según el modelo mecano-cuántico. El límite de la órbita coincide con la zona de mayor probabilidad de encontrar el electrón, pero el electrón también pasa por otros puntos.
