1 - LOS ESTADOS FÍSICOS DE LA MATERIA
Todo en el Universo está formado por materia. La materia se puede encontrar en 3 estados de agregación o estados físicos: sólido, líquido y gaseoso. Solo algunas sustancias pueden hallarse de modo natural en los tres estados, tal es el caso del agua.
Sus propiedades son:
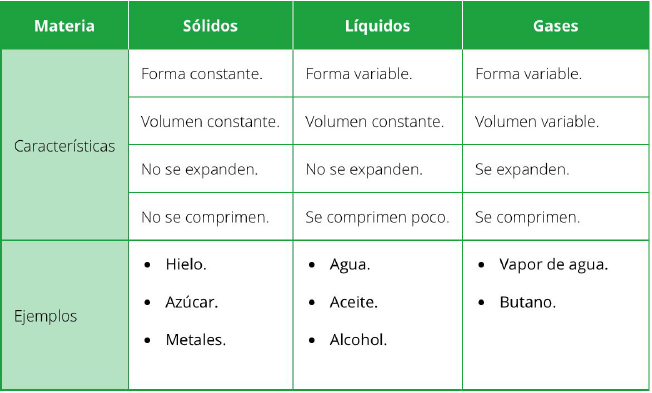
2 - TEORÍA CINÉTICA Y LOS ESTADOS DE LA MATERIA
La teoría cinética nos indica que la materia, sea cual sea su estado, está formada por partículas tan diminutas que no se pueden observar a simple vista y que, además, se encuentran en continuo movimiento.
Ese estado de movimiento depende de la temperatura, cuando calentamos una sustancia, las partículas adquieren más energía y se mueven con mayor velocidad.
